免疫系统作为生物体内最有力的防御屏障,监测细胞和组织的健康状况,识别外源入侵物(如病毒、细菌、微小生物等),执行免疫清除任务,确保生命体安稳的运转。然而,在免疫系统成功解除外源入侵威胁的同时,参与体内药物运输的纳米载体同样会受到免疫系统的干预,导致药物运输障碍。因此,如何帮助纳米载体逃脱机体的免疫清除,延长在生物内的循环时间,已成科研人员的一个研究方向。
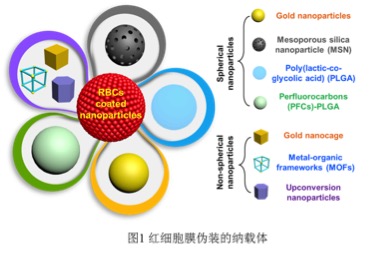
天然红细胞可以自由顺畅的穿梭于血管及各个组织器官之间,而没有遭到免疫攻击,主要由于红细胞膜表面分布着大量的穿膜蛋白(cd47)用于通过免疫系统的识别。科研人员受此启发,使用天然红细胞膜功能化纳米载体的表面。首先将天然红细胞膜分离囊泡化,借助物理挤出、超声融合、微流体加工等手段实现天然红细胞膜在多种纳米载体表面的重构(图1)。经红细胞膜伪装的纳米载体,利用细胞膜复杂的生物成分和功能,成功的“欺骗”机体免疫系统使其视为非入侵源,顺利通过免疫识别,延长在血液中的循环时间,提升病变部位的给药效率。研究还发现,红细胞膜伪涂层不仅能帮助药物载体延长血液循环时间,还能提高其生物相容性,降低在内脏器官中的富集和毒副作用。随后基于红细胞膜伪装材料的研究,科研人员又开发了一系列基于血小板膜、巨噬细胞膜、干细胞膜、癌细胞膜及细菌膜伪装的药物载体,这些新型药物载体在功能上更为多样化,兼顾血液内长循环和药物负载的功能,又集成了主动靶向、免疫抗原、生物防污、清除血液毒素等特性,提升了纳米药物载体在肿瘤诊断与治疗中的应用潜能。
中科国学院化学研究所李峻柏研究员课题组发展了一系列基于细胞膜伪装的纳米载体,显著改善药物分子在体内的递送效率及肿瘤的光治疗效果。近期,该课题组根据这一研究领域的发展状况,促使其它学科的科研人员更深入的了解并推动该领域与其它学科的交叉,近期在《国家科学评论》上发表了的综述文章“cell membranes-covered nanoparticles as biomaterials”。该文章分类总结了细胞膜伪装的纳米载体的研究进展,阐释人工合成纳米药物载体与天然细胞膜相结合的优势与重要性,展望了细胞膜伪的纳米载体在未来临床医学中的应用潜能。
论文相关信息: